あまり知られていないバイオ医薬品会社が後期臨床研究とFDA申請に向けて準備を進めており、商業化の取り組みを主導するために経験豊富なCEOを採用したばかりであるため、新世代の吸入インスリンが市場に近づいています。
ファイザーが失敗した「ボンスタイル」のExubera吸入インスリンが市場から撤退した後、MannKindのAfrezzaがまだ開発中であった後、2010年頃に登場したサンフランシスコ地域のスタートアップであるDanceBiopharmを覚えているかもしれません。このスタートアップは、ほぼ10年間、まったく新しいタイプの吸入インスリンの作成に取り組んできました。
同社は現在、吸入インスリンの世界と新薬の市場投入のビジネス面に精通している元サノフィの幹部であるアン・ウィテカーの最近の採用で注目を集めています。彼女はノースカロライナに拠点を置いており、DanceBiopharmは実際に今後数か月以内に本社を移転する準備をしています。彼らは研究のために西海岸にとどまりますが、幹部は東海岸にいて、ダンスもまもなく中国とイギリスに事務所を開設する準備をします。
「私たちはレーダーから外れています。ステルスモードで作業していると言う人もいるかもしれません。しかし、進捗状況を見ると、注目に値します。これらすべてがまとまって…今こそ、これを前進させる時です」とウィテカー氏は、現在ダンス501(内部仮題)と呼ばれている彼らの小説製品について語っています。
最近の電話チャットで、ウィテカーは彼女がダンスチームに参加した理由と、今後数年間で何が期待できるかについての詳細を教えてくれました。しかし、最初に、この新しい吸入インスリンと、それが患者にどのような利点をもたらすかを見てみましょう。
サイジングアップダンス501、別名吸入インスリン3.0
FDAは、この新しい吸入インスリンの提案された製品ブランド名を検討および承認します。これは、ジェネレーション3.0と呼ばれることもあります。まだDance501として知られているもののプロパティを見てみましょう。

ソフトミスト:吸入可能な白い粉末であるMannKindのAfrezzaインスリンとは異なり、Dance 501はミスト製剤です。つまり、肺の奥深くまで呼吸すると、数滴だけ気化してミストの形になる超濃縮組換えインスリンです。小さなハンドヘルドデバイス。
純粋:他のインスリンとは異なり、この製品は防腐剤を含まないため、実際にインスリンにアレルギーがある障害者の1〜2%にとって重要であり、インスリン部位の発疹からアナフィラキシーショックに至るまでの問題を引き起こします。それは小さなボトルに入った液体の形で提供され、各投与の直前にハンドヘルドデバイスを充填するために使用されます。
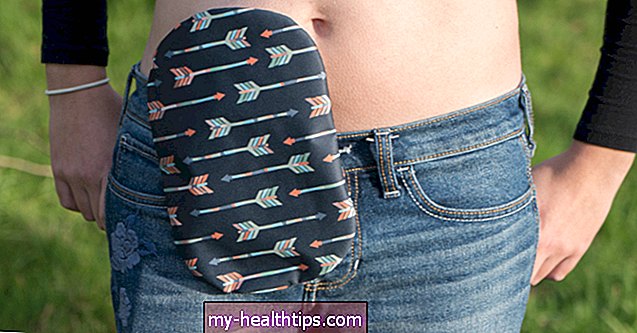
ハンドヘルド吸入器:小さくて使いやすい、ズボンのポケットに収まる昔ながらのブザーとほぼ同じサイズです。これは、私たちが見た初期のプロトタイプとはかなり異なります。 2017年12月、同社は工業デザイナーのPhillips-Medisizeと提携し、改良版を作成しました。その結果、ソフトミストの形で一定サイズの液体インスリンの粒子を生成するように設計された特許取得済みの振動メッシュ技術を使用する電子吸入器が生まれました。 (おもしろい事実:1秒間に120,000の振動があります!)。デバイスは呼吸によって作動し、Dance 501インスリンミストを吸入するのに数回の呼吸しかかかりません。緑色のライトはミストを適切に呼吸していることを示し、その後デバイスの青色のライトが点滅して終了したことを示します。 Whitakerは、最近FDAに最初のデバイスの設計に関する推奨事項を送信し、11月初旬までに規制当局からのフィードバックを聞く予定であると述べています。
次世代吸入器デバイス:第1世代は単3電池のペアを使用しますが、ウィテカー氏によると、第2世代の充電式デバイスで発売後6か月以内に交換される可能性があります。これにより、デバイスのサイズと重量が50%削減され、シャネルのリップスティックチューブのように見えます。
速効性:ウィテカー氏によると、ダンス501は従来のインスリン(特にヒューマログ)よりも速効性があり、アフレッツァ吸入インスリンを改善します。インスリン作用は同じくらい速くピークに達しますが、「長い尾」を持っているため、フォローアップ用量の必要性。フェーズIIの研究では、喉を刺激することなくより自然に肺に入るこの吸入インスリンミストを使用した患者からの低血圧と咳がほとんどないことが示されています。

データの追跡と接続性:吸入器は基本的に小さなコンピューターであるため、服用時の投与量、吸入速度、インスリン投与量、呼吸深度に基づいて実際に肺に入るミストの量などのインスリン使用データを記録します。 Danceはまた、同じデータを含むスマートフォン用のモバイルアプリを立ち上げ、患者が医療提供者と一緒に表示し、最終的にはCGMやデータプラットフォームなどの他のDデバイスに接続することを計画しています。これまでの他の吸入インスリンデバイスは追跡やデバイス接続を提供していなかったため、これらすべてがユニークです。
研究開発のタイミング:Dance 501はエキサイティングかもしれませんが、ここでは忍耐が美徳になります…少なくとも数年後、それ以上ではないにしても、話し合っています。 Danceは過去数年にわたって初期の臨床研究を発表しており、それは2019年半ばになると予想されるものまで進行中のフェーズII試験を続けています。そこから、彼らは2020年に後期段階の第III相試験を開始し、おそらくその年の終わりまでに規制当局の提出時点に到達することを期待しています。もちろん、資金調達はこれらすべての鍵であるため、タイミングはそれによって、また調査が示していることや規制当局が最終的に何を言っているかによって異なる場合があります。
価格設定:ウィテカー氏はまた、価格とコストについてはまだ検討中であると述べています。彼女は、Dance 501が「今日の既存のインスリンの外れ値」になるとは考えていませんが、米国だけでなくグローバル化することで、患者の価格を相殺するのに役立ちます。もちろん、彼らは市場に移動する前に支払人と協力することも計画しています。
液体製剤も:ダンスがこのミスト型の吸入インスリンを開発しているからといって、バイアル/注射器、ペン、またはインスリンポンプで使用するための液体バージョンも検討していないという意味ではありません。現在市場に出回っている伝統的なブランド、ウィテカーは私たちに言います。
非常にエキサイティングですが、もちろん私たちのせっかちな患者は疑問に思わずにはいられません。 この点に到達するのに一体何がそんなに長くかかったのか、そしてなぜ私たちはダンスからこの製品を見るのにまだ何年も離れているのですか?
Whitakerとのチャットでうまく説明されているように、多くの可動部分があります。
DanceBiopharmのCEOであるAnneWhitakerの舞台裏

Whitakerは、糖尿病から腫瘍学、心臓血管、呼吸器、胃腸病学まで、製薬、ライフサイエンス、バイオテクノロジー業界で四半世紀以上の歴史を持っています。彼女の経歴には、KNOW Bio、Novoclem Pharmaceuticals、Inc.、Synta Pharmaceuticals、Inc。の社長兼CEOが含まれます。もちろん、Dコミュニティにとって最も注目すべきは、2011年から2014年までサノフィの北米地域の社長を務めたことです。彼女はすべての製薬、デバイス、および消費者向けヘルスケアビジネスユニットを担当していました。
サノフィでの3年間、ウィテカー氏は、同社がLantusでインスリンの使用を促進しようとし、障害者(糖尿病患者)に実際に処方箋を受け取って適切に使用してもらうことに重点を置いたと述べています。彼女は、以前はインスリンに依存していなかったT2患者の30%だけが、インスリン使用に関する恐怖と混乱のために処方箋を満たしたと言います。
彼女はサノフィにいる間、ダンスについて知っていました。製薬会社の巨人が吸入インスリン市場に参入する準備をしているときに、会社全体のレビューを行いました。 Whitakerは、サノフィがMannKind(Afrezzaのメーカー)と提携することを選択したのは、Danceよりも早く製品を市場に投入する「即時の機会」があるためだと述べています。これは、インスリンの使用を注射剤から遠ざけるための優れた方法と見なされていたと彼女は説明します。しかし、彼女は、同社が障害者の存在感を高めるためにAfrezzaを本来あるべき方法で商品化しておらず、2014年にサノフィを離れることになったと述べています。
元サノフィエグゼクティブは言う:「私は欲求不満でした」
「高等教育機関で製品を発売することはできません」と彼女は言いました。 「正直なところ、遠くから見ていてイライラしました。インスリン吸入の可能性を見たからです。そのため、Danceはこの商品化の経験を持つ人を呼び込みたいと考えていました…私たちは今、商品化の準備に焦点を合わせ始める必要があります。私たちは今そのプロセスを開始しており、発売の準備をしている間、糖尿病コミュニティ全体が私たちからより多くのことを聞くでしょう。」
Whitakerは、南部の「糖尿病ベルト」の真ん中にあるアラバマで育ちました。また、2型と一緒に暮らす叔母と叔父がいて、義父が糖尿病であるため、障害者が感情的なローラーコースターを観察しました。耐え、医師が2型糖尿病患者の脅威としてインスリンを頻繁に使用する方法。
「糖尿病の旅でこの継続的な衰退を経験する前に、それを変えてインスリンの早期使用を促進できることを望んでいます」とウィテカーは言います。 「Danceには、別のオプションを提供できるDance501の製品があります。確かに、ポンプや基礎インスリンに取って代わるものではありませんが、治療のパラダイムの初期の段階にあります。」
もちろん、ウィテカーは、吸入インスリンの可能性について投資家や他の人々を説得しようとするのは困難な戦いであることを知っています。しかし彼女は、Exuberaの失敗、MannKindによるAfrezzaの発売と再発売、そして世界中のテクノロジーと噴霧化の全体的な進化に続いて、過去10年間に変化したことが、以前は不可能だった方法でDance501の舞台を設定したと信じています。 。
ダンスの創設者であるジョン・パットンは、Exuberaの科学的根拠を提供したNektar Therapeuticsの共同創設者兼最高科学責任者であり、現在も取締役会の席でダンスの一員です。 2011年に私たちが話をしたもう1人の幹部は、サマンサミラーです。彼は、商業化の準備をしている間、同社の戦略コンサルタントであり続けています。
興味深いことに、ウィテカー氏によると、Dance Biopharmは2015年後半頃にIPO(新規株式公開)を申請する予定でしたが、サノフィがMannKindのAfrezzaを投棄したとき、その計画は変更されました。代わりに、同社は臨床研究を推進し、デバイスをより洗練された洗練されたものに改訂しました。
吸入可能なもののための熟した環境
時代は確かに変わりました—人々が吸入可能なものの考えにもっとオープンであると信じるダンスの理由を与えます。
最近、電子タバコとアークが世界中で一般的になり、ウィテカーは、医療用噴霧が爆発的に増え、世界的に受け入れられるようになっていると指摘しています。彼女は、米国の医薬品市場の8%がステロイド薬にハンドヘルドネブライザーを使用しているのに対し、ヨーロッパでは12%、中国では20%であると述べています。
「Dance501を市場に投入し、商品化する可能性はあります。ダンスのタイミングは正しいです」とウィテカーは言います。
製造コストは確かにウィテカーの心の関心事であり、ExuberaとAfrezzaが製造して市場に出すのにどれだけのコストがかかるかをよく知っています– 10億ドル以上(!)しかし、ダンスはそれらのコストのほんの一部しか費やすことができないと彼女は言います、彼らは、海外で米国向けのDance 501を製造するために、FDAの検査を受けた工場を持つために、アジア最大のインスリンメーカーと協力しているからです。
「また、安全性、有効性、および患者の使用に関するデータが豊富にあるため、私たちの前に来た吸入インスリンの肩に立っていることも幸運です」と彼女は付け加えます。
Whitakerはまた、同社の研究および製造チームはサンフランシスコ地域にとどまり、Dance Biopharmの商業本部は今後6〜9か月以内にノースカロライナ州のリサーチトライアングルパークに移転し、それまでは営業していると付け加えています。リモートで。彼らはまた、ヨーロッパのオフィスと中国のオフィスを開設することを計画していると彼女は言った。
吸入インスリンは牽引力を獲得していますか?
私たちは、この新製品の可能性について慎重に楽観的です。例としてMannKindのAfrezzaを取り上げます。 '私の それを使用して、それを愛してください。しかし、実際には、MannKindは苦戦しており、処方数は依然として少なく、多くの医師は2015年以降市場に出回っている粉末製剤に依然として一般的に躊躇しています。インスリン市場は競争が激しく、気まぐれな市場であり、何も保証されていません(事実を除いて) T1Dを使用する障害者はそれなしでは行けません!)。
それでも、これらすべてを念頭に置いて、ダンスが市場に出て、Exuberaが失敗し、MannKindが強力な足場を築くのに苦労している場所で成功できることを願っています。
更新:2019年9月、同社はAeramiTherapeuticsとしてブランド名を変更しました。




-with-country-music-star-eric-paslay.jpg)